Szalenie istotny temat.
Nawrót po leczeniu miejscowym raka gruczołu krokowego – fakty zamiast mitów !
To zagadnienie było przedmiotem naszej najnowszej publikacji w Technology in Cancer Research & Treatment, w której pokazujemy, jakie realne możliwości leczenia istnieją po wznowie po radioterapii — i jakie są ich wyniki.
Zanim jednak przejdziemy do leczenia ratunkowego, warto uczciwie odpowiedzieć na jedno pytanie:
jak często w ogóle dochodzi do niepowodzeń po leczeniu miejscowym?
Optymalnie i świadomie wybrana przez pacjenta metoda leczenia raka gruczołu krokowego — a taka może być podjęta wyłącznie po rozmowie zarówno z urologiem, jak i radioterapeutą onkologicznym — jest decyzją strategiczną. To wybór, który determinuje ścieżkę terapeutyczną i jakość życia chorego na kolejne 10–15 lat.
W debacie „operacja czy radioterapia?” często słyszymy, że zabieg chirurgiczny jest rozwiązaniem definitywnym. Znacznie rzadziej mówi się otwarcie o tym, że także prostatektomia radykalna wiąże się z istotnym odsetkiem niepowodzeń biologicznych — i to wcale nie marginalnym.
Zacznijmy więc od faktów. Twardych danych naukowych.
Dodatnie marginesy chirurgiczne po prostatektomii występują w zakresie 11–37% przypadków, zależnie od zaawansowania i grupy ryzyka [1–3]. W erze chirurgii robotowej często podkreśla się poprawę precyzji zabiegu. Jednak nawet w dużych, wysokowolumenowych ośrodkach robotowych dodatni margines chirurgiczny po RARP występuje u około 22% pacjentów.
Co więcej, w grupie pośredniego ryzyka obecność rozległego dodatniego marginesu wiązała się z 57,5% ryzykiem nawrotu biochemicznego, a 40% tych pacjentów wymagało radioterapii ratunkowej. W grupie wysokiego ryzyka sytuacja była jeszcze bardziej niepokojąca — nawrotu biochemicznego doświadczało do 90–100% pacjentów z dodatnim marginesem, a większość wymagała leczenia uzupełniającego [3].
To pokazuje jasno:
Robot nie zmienia biologii nowotworu.
Kolejnym problemem jest tzw. PSA persistence — utrzymywanie się wykrywalnego PSA po prostatektomii, które w praktyce uruchamia kaskadę dalszego leczenia (ratunkowa radioterapia ± ADT).
W dużym badaniu kohortowym obejmującym 43 298 pacjentów persistent PSA (zdefiniowane jako ≥0,10 ng/mL przy pierwszym oznaczeniu po operacji) stwierdzono u 4,7% chorych, przy medianie czasu pierwszego oznaczenia 2,17 miesiąca. Co szczególnie ważne, w grupie z wysokim PSA przedoperacyjnym odsetek ten był wielokrotnie wyższy: przy PSA >20 ng/mL persistent PSA dotyczyło 14,0% pacjentów (vs 3,6% przy PSA ≤20 ng/mL) [4].
Jest to wczesne niepowodzenie biologiczne, które bardzo często prowadzi do konieczności wdrożenia radioterapii ratunkowej, nierzadko w skojarzeniu z hormonoterapią.
Jeżeli spojrzymy na dłuższą perspektywę, odsetek niepowodzeń biologicznych po prostatektomii jest istotny. W analizach klinicznych opartych na dużych kohortach około 30–50% pacjentów doświadcza nawrotu biochemicznego w ciągu 10 lat po radykalnej prostatektomii, co oznacza, że co drugi-trzeci pacjent wraca do ścieżki dalszego leczenia, takiej jak radioterapia ratunkowa czy terapia systemowa [5,6].
Radioterapia również nie jest wolna od niepowodzeń.
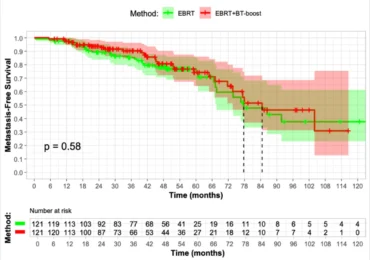
W metaanalizie LEVIATHAN (MARCAP consortium, 18 randomizowanych badań) lokalne niepowodzenie po radioterapii wystąpiło u około 13% pacjentów z grupy high-risk oraz 7,2% z grupy intermediate-risk, przy medianie obserwacji około 11 lat [8]. Co istotne, lokalna wznowa była silnie związana z późniejszym ryzykiem przerzutów i pogorszeniem rokowania.
Kluczowa różnica polega jednak na czymś innym.
Wciąż funkcjonuje mit, że po nawrocie po radioterapii „nic już nie można zrobić” i pozostaje wyłącznie leczenie systemowe. Aktualne dane naukowe temu przeczą!
W ostatnim czasie ukazał się bardzo wartościowy przegląd GEC-ESTRO dotyczący przede wszystkim reiradiacji przy użyciu brachyterapii [7]. Od czasu jego publikacji pojawiły się jednak kolejne metaanalizy obejmujące znacznie większą liczbę pacjentów, pozwalające lepiej zrozumieć realne wyniki leczenia ratunkowego — brachyterapii LDR, brachyterapii HDR, SBRT.
Perspektywę wynikającą z tych analiz omówiliśmy w naszej, już wspomnianej, najnowszej publikacji „Balancing Efficacy and Toxicity in Salvage Brachytherapy and SBRT for Radio-Recurrent Prostate Cancer: Insights Beyond the UroGEC Review”, która właśnie ukazała się na łamach Technology in Cancer Research and Treatment [8].
Publikacja ta w sposób syntetyczny pokazuje, czego można się spodziewać po różnych modalnościach reiradiacji i jest niezwykle pomocna w rozmowie z pacjentami rozważającymi leczenie ratunkowe, ale i wybór metody leczenia na początku swojej ścieżki terapeutycznej !
W najnowszych metaanalizach ratunkowa brachyterapia HDR osiągnęła około 52% 5-letniego RFS (czas wolnego od nawrotu) przy bardzo niskim odsetku istotnej nietolerancji ze strony przewodu pokarmowego (<1%) i około 5% istotnej nietolerancji ze strony układu moczowego.
Brachyterapia LDR osiągała najlepsze wyniki spośród modalności radioterapeutycznych — 63% 5-letniego RFS, jednak kosztem wyższej nietolerancji ze strony układu moczowo-płciowego.
Ratunkowa reiradiacja przy użyciu SBRT osiągnęła 40% 5-letniego RFS przy akceptowalnym profilu bezpieczeństwa.
Dlaczego ta dyskusja jest tak ważna?
Ponieważ w praktyce klinicznej bardzo często obserwujemy sekwencję:
operacja → radioterapia ratunkowa → hormonoterapia.
W efekcie kumulujemy działania niepożądane kilku metod leczenia, zwiększając ryzyko nietrzymania moczu, zaburzeń erekcji, powikłań ze strony odbytnicy oraz konsekwencji metabolicznych terapii systemowej.
Świadomy onkolog — niezależnie od specjalizacji — wie, że celem nowoczesnej onkologii nie jest maksymalizacja liczby wykonanych zabiegów. Celem jest minimalizacja ryzyka kaskady terapeutycznej i świadome planowanie sekwencji leczenia w oparciu o biologię choroby, tak aby jak najmniej obciążyć pacjenta terapią i jej działaniami niepożądanymi oraz zapewnić możliwie najlepszą jakość życia w perspektywie 10–20 lat.
Terapia raka gruczołu krokowego to nie kwestia ideologii!
To kwestia strategii !
1. Pfitzenmaier J, Pahernik S, Tremmel T, Haferkamp A, Buse S, Hohenfellner M. Positive surgical margins after radical prostatectomy: do they have an impact on biochemical or clinical progression? BJU Int. 2008 Nov;102(10):1413-8. doi: 10.1111/j.1464-410X.2008.07791.x. Epub 2008 Jun 4. PMID: 18537951.
2. Yang, CW., Wang, HH., Hassouna, M.F. et al. Prediction of a positive surgical margin and biochemical recurrence after robot-assisted radical prostatectomy. Sci Rep 11, 14329 (2021).
Link
3. Hagman A, Lantz A, Grannas D, Carlsson S, Akre O, Olsson M, Egevad L, Höijer J, Wiklund P. Positive surgical margin and oncological outcomes after robot-assisted radical prostatectomy in different Cancer of the Prostate Risk Assessment risk groups. BJU Int. 2025 Jul;136(1):135-142. doi: 10.1111/bju.16732. Epub 2025 Apr 24. PMID: 40275471; PMCID: PMC12134417.
4. Tilki D, Chen MH, Wu J, Huland H, Graefen M, Trock BJ, Han M, D’Amico AV. Persistent Prostate-Specific Antigen Following Radical Prostatectomy for Prostate Cancer and Mortality Risk. JAMA Oncol. 2025 May 1;11(5):502-510. doi: 10.1001/jamaoncol.2025.0110. PMID: 40080000; PMCID: PMC11907358.
5. Preisser F, Incesu RB, Rajwa P, Chlosta M, Nohe F, Ahmed M, Abreu AL, Cacciamani G, Ribeiro L, Kretschmer A, Westhofen T, Smith JA, Steuber T, Calleris G, Raskin Y, Gontero P, Joniau S, Sanchez-Salas R, Shariat SF, Gill I, Karnes RJ, Cathcart P, Van Der Poel H, Marra G, Tilki D. Impact of persistent PSA after salvage radical prostatectomy: a multicenter study. Prostate Cancer Prostatic Dis. 2024 Dec;27(4):686-692. doi: 10.1038/s41391-023-00728-5. Epub 2023 Oct 6. PMID: 37803241; PMCID: PMC11543598.
5. Shore, N.D., Moul, J.W., Pienta, K.J. et al. Biochemical recurrence in patients with prostate cancer after primary definitive therapy: treatment based on risk stratification. Prostate Cancer Prostatic Dis 27, 192–201 (2024).
6. Menon M, Bhandari M, Gupta N, Lane Z, Peabody JO, Rogers CG, Sammon J, Siddiqui SA, Diaz M. Biochemical recurrence following robot-assisted radical prostatectomy: analysis of 1384 patients with a median 5-year follow-up. Eur Urol. 2010 Dec;58(6):838-46. doi: 10.1016/j.eururo.2010.09.010. Epub 2010 Sep 17. PMID: 20869162.
7. Gomez-Iturriaga A, Tselis N, Willisch P, Guix B, Buchser D, Chyrek A, Monge RM, Sarria GR, Strnad V, Wojcieszek P, Hoskin P, Strouthos I. Salvage brachytherapy for recurrent prostate cancer after radiotherapy: An expert-endorsed review by uroGEC. Radiother Oncol. 2025 Sep;210:111042. doi: 10.1016/j.radonc.2025.111042. Epub 2025 Jul 8. PMID: 40639765.
8. Bilski M, Fijuth J, Kuncman Ł. Balancing Efficacy and Toxicity in Salvage Brachytherapy and SBRT for Radio-Recurrent Prostate Cancer: Insights Beyond the UroGEC Review. Technol Cancer Res Treat. 2026 Jan-Dec;25:15330338261415791. doi: 10.1177/15330338261415791. Epub 2026 Jan 27. PMID: 41591930; PMCID: PMC12847645.